
INTRODUCTION TO THE INSTITUTE

用于實(shí)體腫瘤內(nèi)的納米顆粒富集進(jìn)而增效抗腫瘤治療——超聲聯(lián)合仿病毒表面拓?fù)浣Y(jié)構(gòu)的給藥策略
文章標(biāo)題:Marriage of Virus-Mimic Surface Topology and Microbubble-Assisted Ultrasound for Enhanced Intratumor
Accumulation and Improved Cancer Theranostics
第一作者:Zheying Meng, Yang Zhang, E Shen
通訊作者:Wenkun Bai,* Bing Hu,* Wenxing Wang,* and Yuanyi Zheng
DOI:https://doi.org/10.1002/advs.202004670
論文導(dǎo)讀:
納米顆粒在實(shí)體腫瘤內(nèi)的低遞送效率導(dǎo)致治療效果降低和副作用加重是納米治療劑臨床轉(zhuǎn)化的關(guān)鍵難題。最近的Meta分析表明,2015年-2018年的新近研究與2005年-2015年的所有研究相比,納米顆粒的實(shí)體腫瘤遞送效率并沒有統(tǒng)計(jì)學(xué)意義的改善。上海交通大學(xué)附屬第六人民醫(yī)院鄭元義課題組聯(lián)合復(fù)旦大學(xué)化學(xué)院王文興課題組針對(duì)這一關(guān)鍵科學(xué)問題進(jìn)行了探討,通過優(yōu)化納米顆粒表面結(jié)構(gòu)為仿病毒結(jié)構(gòu),以增強(qiáng)納米顆粒表面粗糙程度、促進(jìn)腫瘤細(xì)胞的攝取;同時(shí)聯(lián)合使用微泡輔助低頻超聲(MAUS)作為被動(dòng)靶向手段,提高生物屏障的通透性,顯著提高納米顆粒在實(shí)體腫瘤的遞送和滲透。這項(xiàng)策略在前列腺癌的平均遞送效率達(dá)6.84%,顯著高于目前報(bào)道的最高水平1.42%。
研究進(jìn)展:
微泡輔助低頻超聲(microbubble-assisted low-frequency ultrasound,MAUS)技術(shù)具備安全、非侵入性的優(yōu)勢(shì),利用超聲激發(fā)微泡產(chǎn)生的聲空化效應(yīng)能夠一過性提高生物膜(如血管內(nèi)皮和細(xì)胞膜)的滲透性。MAUS已被用于增強(qiáng)基因或藥物在眾多疾病模型的靶向遞送,如腦卒中、心血管疾病和腫瘤。然而,納米顆粒作為治療劑本身或作為基因及藥物的載體,目前在實(shí)體腫瘤的遞送效率極低,如在前列腺癌的遞送效率最高的記錄僅為1.42%。MAUS是否能夠提高納米顆粒在實(shí)體腫瘤的富集具有探索價(jià)值。該研究使用了500 kHz的低頻超聲,而不是大多數(shù)當(dāng)前研究中大多采用的1 MHz超聲。眾所周知,低頻超聲具有較高的組織穿透力的優(yōu)勢(shì),這可以進(jìn)一步促進(jìn)納米粒子在深部腫瘤中的遞送。此外,低頻超聲具備更低的聲壓閾值,更容易觸發(fā)聲空化效應(yīng),有助于一過性提高生物膜的滲透性。
從納米顆粒的固有性質(zhì)的角度來看,當(dāng)納米粒子具有相似的表面積、電荷和表面涂層時(shí),表面拓?fù)浣Y(jié)構(gòu)可能會(huì)嚴(yán)重影響納米顆粒的外滲能力。表面粗糙度可以大大增加“納米顆粒-生物界面"相互作用的表面積,降低相互排斥作用,從而促進(jìn)粘附和細(xì)胞吞噬。
因此,研究者假設(shè)仿病毒粗糙表面拓?fù)浣Y(jié)構(gòu)的納米顆粒可以增加的納米顆粒-生物屏障界面的相互作用。最終該研究成功采用單膠束外延生長(zhǎng)的方法制備了多功能的納米顆粒,即仿病毒結(jié)構(gòu)的二氧化硅包裹內(nèi)部磁性Fe3O4的特殊核殼結(jié)構(gòu)納米顆粒MVSN-IR825,其制備過程步驟示意圖如圖1A。MVSN-IR825的TEM圖像(1B), SEM圖像(1C, 1D), 尺寸分布(1E)和紫外-可見-近紅外吸收光譜(1F)如圖1所示。同時(shí)合成了光滑表面、介孔表面的MSSN-IR825、MMSN-IR825作為對(duì)照,三種粒徑大致相仿、IR825接枝率大致相同。
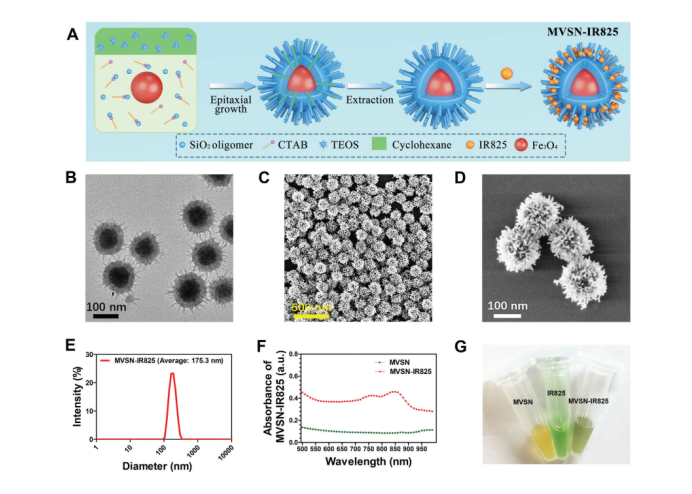
圖1 MVSN-IR828的制備和表征
隨后通過細(xì)胞攝取實(shí)驗(yàn)證實(shí),與MSSN-IR825、MMSN-IR825相比,MVSN-IR825具有更高的細(xì)胞攝取率;MAUS可以進(jìn)一步增加前列腺癌細(xì)胞攝取。如圖2所示,細(xì)胞核呈現(xiàn)DAPI染色后的紫色熒光,納米顆粒呈現(xiàn)FITC標(biāo)記后的綠色熒光,在相同的孵育時(shí)間內(nèi),MVSN-IR825組顯示出比MSSN-IR825和MMSN-IR825更多細(xì)胞內(nèi)綠色熒光。除此之外,流式細(xì)胞術(shù)檢測(cè)結(jié)果(圖2B 2D)也表明,MVSN-IR825組比MSSN-IR825組和MMSN-IR825組顯示出更有效的細(xì)胞內(nèi)化;MAUS可以進(jìn)一步增加前列腺癌細(xì)胞攝取。
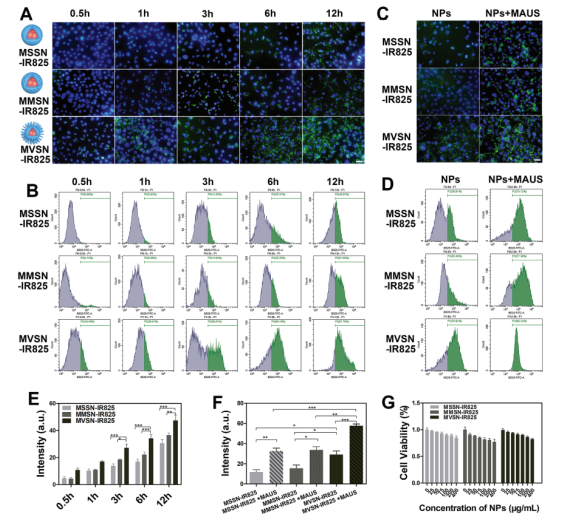
圖2 細(xì)胞攝取實(shí)驗(yàn)
基于細(xì)胞水平實(shí)驗(yàn)已證實(shí)了仿病毒結(jié)構(gòu)納米顆粒聯(lián)合MAUS可以增加前列腺癌細(xì)胞攝取納米顆粒,隨后研究進(jìn)一步在體內(nèi)實(shí)驗(yàn)進(jìn)行驗(yàn)證。為了比較不同表面結(jié)構(gòu)納米顆粒、聯(lián)合使用MAUS是否促進(jìn)納米顆粒在實(shí)體腫瘤內(nèi)的富集,改研究建立PC-3皮下移植瘤、PC-3原位瘤的模型,使用多種成像模式包括PAI、FI in vivo、MRI進(jìn)行驗(yàn)證(如圖3),由于MVSN-IR825納米顆粒因?yàn)镮R825的存在,可以進(jìn)行PAI、FI in vivo;由于內(nèi)部含有Fe3O4核,可以進(jìn)行MRI的T2加權(quán)成像,因此本章在PAI、FI in vivo、MRI多種模態(tài)成像下驗(yàn)證了MVSN-IR825優(yōu)于MSSN-IR825、MMSN-IR825的腫瘤內(nèi)富集效果,以及聯(lián)合使用MAUS后實(shí)體瘤內(nèi)的納米顆粒富集進(jìn)一步增加。
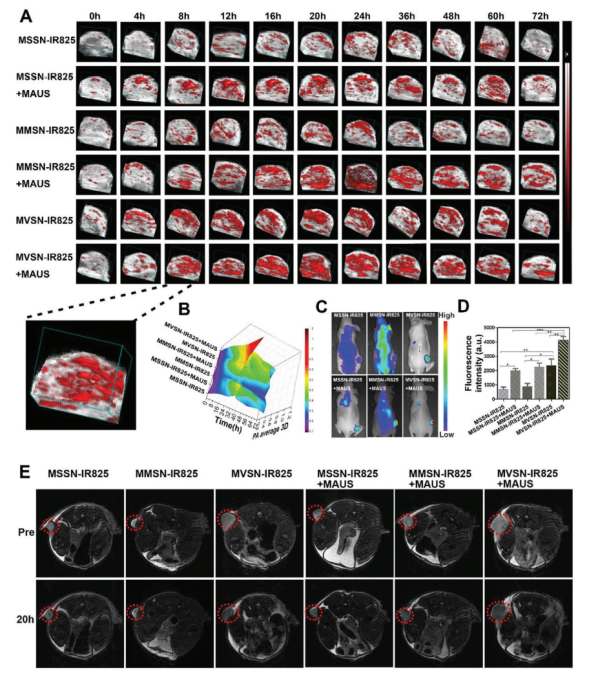
圖3 多種成像方法監(jiān)測(cè)PC-3異種移植荷瘤小鼠中納米顆粒的富集
隨后進(jìn)一步從組織學(xué)水平進(jìn)行普魯士藍(lán)染色顯示鐵沉積和分布進(jìn)一步證實(shí)了MVSN-IR825聯(lián)合MAUS可以促進(jìn)納米顆粒突破腫瘤血管、提高納米顆粒在深部腫瘤間質(zhì)的滲透(如圖4 A)。定量的ICP分析結(jié)果表明MVSN-IR825聯(lián)合MAUS可使納米顆粒的腫瘤遞送效率提高至6.82%,遠(yuǎn)高于目前研究報(bào)道前列腺癌納米顆粒富集的最大遞送效率1.42%(如圖4 B)。同時(shí)影像學(xué)結(jié)果以及ICP的多個(gè)時(shí)間點(diǎn)監(jiān)測(cè)結(jié)果表明了尾靜脈注射20小時(shí)后實(shí)體瘤內(nèi)富集達(dá)到高峰,這為后續(xù)在體抗腫瘤治療研究提供了最有效治療時(shí)間點(diǎn)。MVSN-IR825因?yàn)閮?nèi)部Fe3O4核而具備類過氧化氫酶活性,可與H2O2反應(yīng)產(chǎn)生氧氣。這為后續(xù)MVSN-IR825的光動(dòng)力和聲動(dòng)力治療提供了重要保證(如圖4 C, 4 D, 4 E)。
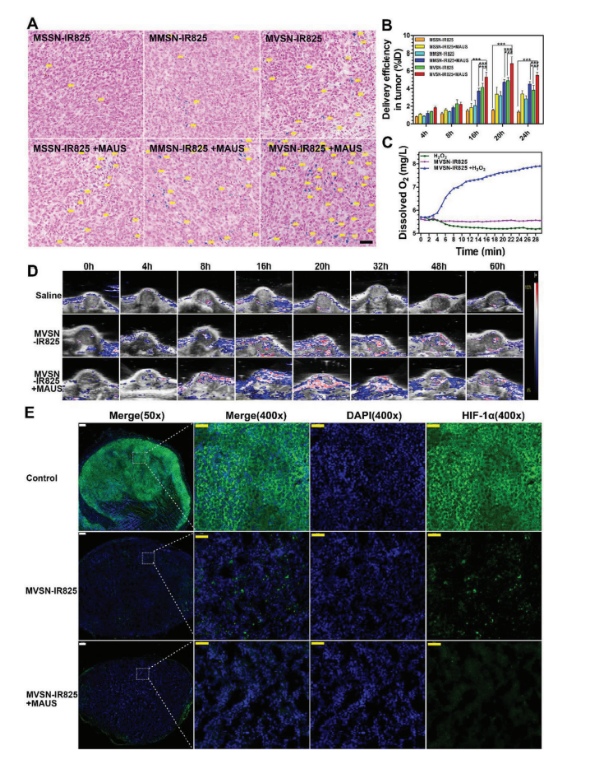
圖4 腫瘤內(nèi)納米顆粒的富集以及腫瘤乏氧狀態(tài)的改善
然后研究從體外水平探索了MVSN-IR825的光熱、光動(dòng)力、聲動(dòng)力多模式抗腫瘤治療的能力。首先MVSN-IR825具備良好、穩(wěn)定的光熱轉(zhuǎn)換能力(圖5 A, 5 B)。其次,體外ESR檢測(cè)活性氧產(chǎn)生的實(shí)驗(yàn)證實(shí)了MVSN-IR825可在激光和超聲的輻照下產(chǎn)生單線態(tài)氧,尤其在氧氣輔助下可明顯提高單線態(tài)氧的產(chǎn)生(圖5 C, D)。細(xì)胞水平DCFH-DA染色進(jìn)一步驗(yàn)證了激光和超聲輻照下細(xì)胞內(nèi)活性氧的產(chǎn)生;而激光和超聲的聯(lián)合輻照可進(jìn)一步提高細(xì)胞內(nèi)活性氧水平(圖5 G)。CCK-8實(shí)驗(yàn)和活死染色進(jìn)一步證實(shí)了激光和超聲聯(lián)合輻照具有最佳的前列腺癌細(xì)胞治療效果,激光輻照和超聲輻照使用的先后順序?qū)骨傲邢侔┘?xì)胞治療效果沒有明顯差異(圖5 H)。因此,細(xì)胞水平證實(shí)了激光輻照細(xì)胞時(shí)可通過光熱和光動(dòng)力兩種方式殺傷前列腺癌細(xì)胞。
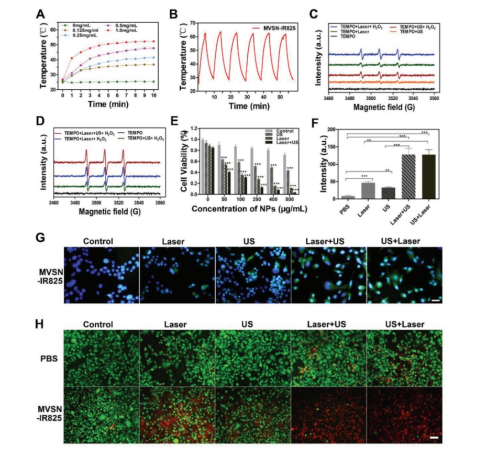
圖5 MVSN-IR825體外的抗腫瘤治療
基于前期實(shí)驗(yàn)結(jié)果,研究采用MVSN-IR825聯(lián)合MAUS尾靜脈給藥20小時(shí)后開始治療的方案,激光輻照皮下瘤、原位瘤均得到明顯的升溫表明MVSN-IR825在實(shí)體瘤內(nèi)的有效富集。超聲造影(圖6 A)、生物發(fā)光成像(圖6 B)結(jié)果表明單獨(dú)激光或超聲輻照可部分抑制腫瘤活性,但是激光和超聲聯(lián)合輻照可完全抑制腫瘤活性。同時(shí)DHE染色結(jié)果(圖6 C)表明激光和超聲輻照的皮下瘤和原位瘤組織內(nèi)產(chǎn)生活性氧,并且激光和超聲聯(lián)合輻照后活性氧產(chǎn)生更多,表明實(shí)體瘤內(nèi)富集的MVSN-IR825可通過光動(dòng)力治療、聲動(dòng)力治療抑制前列腺癌實(shí)體瘤。此外,Ki67染色和Tunel染色結(jié)果(圖6 D)也反映了組織學(xué)水平抗腫瘤治療的有效性。腫瘤大小的監(jiān)測(cè)結(jié)果(圖6 E)表明單獨(dú)激光輻照、單獨(dú)超聲輻照可在一定程度抑制前列腺癌實(shí)體瘤的生長(zhǎng),但是存在殘余腫瘤繼續(xù)生長(zhǎng)的現(xiàn)象;激光和超聲聯(lián)合輻照皮下瘤和原位瘤,可完全抑制腫瘤。該研究從在體水平論證了近紅外激光和低頻超聲聯(lián)合輻照MVSN-IR825可通過光熱、光動(dòng)力、聲動(dòng)力三種模式完全抑制前列腺癌實(shí)體瘤。
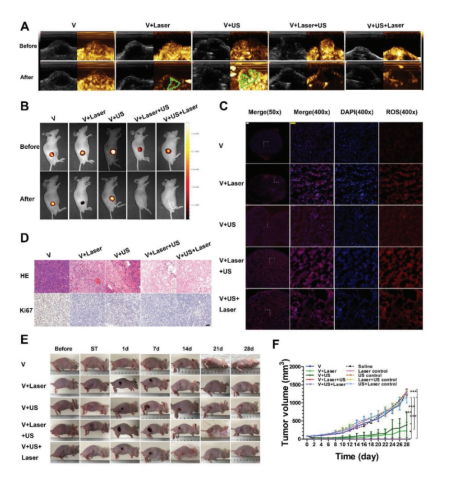
圖6 PC-3皮下荷瘤小鼠的體內(nèi)治療效果
總結(jié)與展望:
上海交通大學(xué)附屬第六人民醫(yī)院上海超聲醫(yī)學(xué)研究所(超聲醫(yī)學(xué)科)聯(lián)合復(fù)旦大學(xué)化學(xué)院王文興課題組針對(duì)納米顆粒在腫瘤內(nèi)靶向效果差、富集少的關(guān)鍵科學(xué)問題,本研究從納米顆粒自身表面結(jié)構(gòu)優(yōu)化的角度合成了仿病毒結(jié)構(gòu)的納米顆粒MVSN-IR825,同時(shí)合成了另外兩種不同表面結(jié)構(gòu)納米顆粒MSSN-IR825、MMSN-IR825作為對(duì)照;從外源性被動(dòng)靶向技術(shù)的角度引入了MAUS的輔助。通過優(yōu)化納米顆粒為仿病毒結(jié)構(gòu)以增強(qiáng)納米粒表面粗糙程度;聯(lián)合使用微泡輔助低頻超聲(MAUS)作為被動(dòng)靶向手段,提高生物屏障的通透性,提高納米顆粒在實(shí)體前列腺腫瘤的富集。最終研究制備仿病毒結(jié)構(gòu)的多功能納米顆粒MVSN-IR825,研究主要使用PC-3異種腫瘤進(jìn)行深度研究。為了進(jìn)一步證實(shí)此項(xiàng)策略的有效性,該研究在體外AGS胃癌細(xì)胞和143B骨肉瘤細(xì)胞,以及在體內(nèi)PC-3原位腫瘤和143B異種腫瘤進(jìn)行進(jìn)一步驗(yàn)證。這項(xiàng)工作從體外、細(xì)胞、動(dòng)物多水平,通過影像學(xué)、組織學(xué)、多種動(dòng)物模型等多種方法清楚地證明 “內(nèi)在+外在優(yōu)勢(shì)”策略極大地改善了納米粒子在腫瘤內(nèi)的滲透和分布,增強(qiáng)了癌癥的治療效果。本研究設(shè)計(jì)的診療一體化的納米顆粒為探索前列腺癌的臨床診療方向提供依據(jù),同時(shí)也為腫瘤納米醫(yī)學(xué)中的關(guān)鍵瓶頸問題提供了新的解決思路。
論文信息:
Marriage of Virus-mimic Surface Topology and Microbubble-assisted Ultrasound for Enhanced Intratumor Accumulation and Improved Cancer Theranostics
Zheying Meng, Yang Zhang, E Shen, Wei Li, Yanjie Wang, Krishnan Sathiyamoorthy, Wei Gao, Michael C. Kolios, Wenkun Bai*, Bing Hu*, Wenxing Wang*, Yuanyi Zheng*
Advanced Science
DOI: 10.1002/advs.202004670
原文鏈接:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202004670